国家药监局已批准29个新冠病毒抗原检测试剂
来源 : 人民网
时间 : 2022-04-20
A+
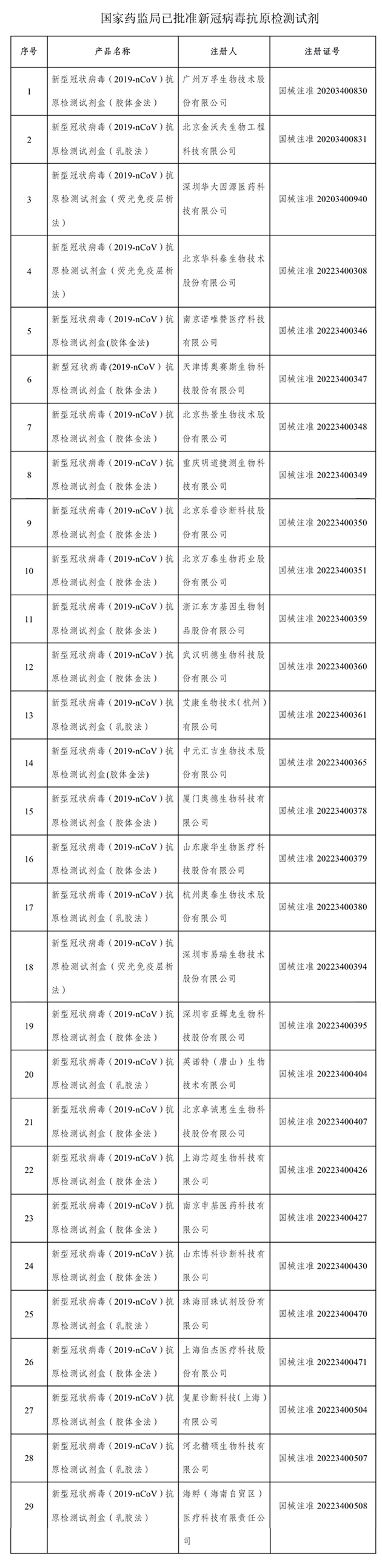
据国家药监局官网消息,4月20日,国家药监局再次审查批准2个新冠病毒抗原检测试剂产品。截至4月20日,国家药监局已批准29个新冠病毒抗原检测试剂产品。
国家药监局表示,新冠病毒抗原检测试剂适用于《新冠病毒抗原检测应用方案(试行)》(联防联控机制综发〔2022〕21号)规定的人群。药品监督管理部门将加强相关产品上市后监管,保护患者用械安全。
资料显示,3月12日,国家药监局发布通告,批准南京诺唯赞、北京金沃夫、深圳华大因源、广州万孚生物、北京华科泰生物的新冠病毒抗原产品自测应用申请变更。
3月13日,国家药监局批准5家新冠病毒抗原产品的注册申请,分别为万泰生物、热景生物、天津博奥赛斯生物、重庆明道捷测生物和北京乐普诊断。
3月15日,国家药监局批准2家新冠病毒抗原产品的注册申请,分别为浙江东方生物、武汉明德生物。
3月16日,国家药监局批准艾康生物技术(杭州)有限公司的新冠病毒抗原产品的注册申请。
3月17日,国家药监局批准中元汇吉生物技术股份有限公司的新冠病毒抗原产品的注册申请。
3月18日,国家药监局批准3家新冠病毒抗原产品的注册申请,分别为厦门奥德生物、山东康华生物、杭州奥泰生物。
3月23日,国家药监局批准2家新冠病毒抗原产品的注册申请,分别为深圳易瑞生物、深圳亚辉龙生物。
3月29日,国家药监局批准英诺特(唐山)生物技术有限公司的新冠病毒抗原产品的注册申请。
3月30日,国家药监局批准北京卓诚惠生生物科技股份有限公司的新冠病毒抗原产品的注册申请。
4月1日,国家药监局批准2家新冠病毒抗原产品的注册申请,分别为上海芯超生物、南京申基医药。
4月2日,国家药监局批准山东博科诊断科技有限公司的新冠病毒抗原产品的注册申请。
4月12日,国家药监局批准2家新冠病毒抗原产品的注册申请,分别为珠海丽珠试剂、上海伯杰医疗。
4月13日,国家药监局批准复星诊断科技(上海)有限公司的新冠病毒抗原产品的注册申请。
国家药监局官网截图